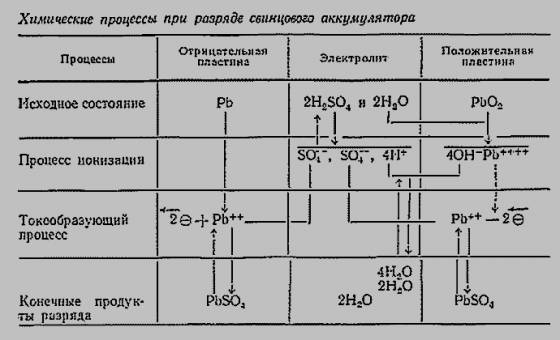
Свинцовые аккумуляторы являются
вторичными химическими источниками тока, которые могут использоваться
многократно. Активные материалы, израсходованные в процессе разряда,
восстанавливаются при последующем заряде.
Химический источник
тока представляет собой совокупность реагентов (окислителя и
восстановителя) и электролита. Восстановитель (отрицательный электрод)
электрохимической системы в процессе токообразующей реакции отдает
электроны и окисляется, а окислитель (положительный электрод), принимая электроны -
восстанавливается.
Электролитом, как правило, является
жидкое химическое соединение, обладающее хорошей ионной и малой
электронной проводимостью. В свинцовом аккумуляторе в токообразующих
процессах участвуют двуокись свинца (диоксид свинца) РЬО2 (окислитель) положительного
электрода, губчатый свинец РЬ (восстановитель) отрицательного
электрода и электролит (водный раствор серной кислоты H2S04).
Активные
вещества электродов представляют собой относительно жесткую пористую
электронопроводящую массу с диаметром пор 1,5 мкм у РЬО2 и 5-10 мкм у губчатого свинца.
Объемная пористость активных веществ в заряженном состоянии - около 50%.
Часть
серной кислоты в электролите диссоциирована (растворена) на
положительные ионы водорода Н+
и отрицательные ионы кислотного остатка SO42-. Губчатый
свинец при разряде аккумулятора выделяет в электролит положительные ионы
двухвалентного свинца РЬ2+.
Избыточные электроны отрицательного электрода по внешнему участку
замкнутой электрической цепи перемещаются к положительному электроду,
где восстанавливают четырехвалентные ионы свинца РЬ4+ до двухвалентного свинца РЬ2+.
Положительные ионы свинца РЬ2+ соединяются с отрицательными ионами
кислотного остатка SO42-, образуя на обоих электродах
сернокислый свинец РЬSО4
(сульфат свинца).
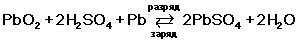
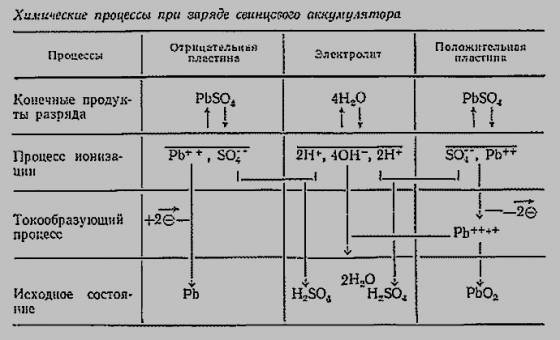
При подключении
аккумулятора к зарядному устройству электроны движутся к отрицательному
электроду, нейтрализуя двухвалентные ионы свинца РЬ2+. На электроде выделяется губчатый
свинец РЬ. Отдавая под влиянием напряжения внешнего источника
тока по два электрона, двухвалентные ионы свинца РЬ2+ у положительного электрода окисляются в
четырехвалентные ионы РЬ4+.
Через промежуточные реакции ионы РЬ4+
соединяются с двумя ионами кислорода и образуют двуокись свинца РЬO2.